Ácido metanoico
| Ácido fórmico Alerta sobre risco à saúde | |
|---|---|
|

|
| Nome IUPAC | Ácido metanoico Ácido fórmico |
| Outros nomes | Hydrogen carboxylic acid Formylic acid Aminic acid |
| Identificadores | |
| Número CAS | |
| PubChem | |
| Número EINECS | |
| ChemSpider | |
| ChEBI | |
| Número RTECS | LQ4900000 |
| Código ATC | P53 |
| SMILES |
|
| InChI | 1/CH2O2/c2-1-3/h1H,(H,2,3)/f/h2H
|
| Propriedades | |
| Fórmula química | CH2O2 |
| Massa molar | 46.01 g mol-1 |
| Aparência | líquido incolor[1] |
| Densidade | 1,22 g·cm?3, líquido (20 °C)[2] |
| Ponto de fusão |
8.3 °C [3] |
| Ponto de ebulição |
101 °C [3] |
| Solubilidade em água | 1000 g/l a 25 °C [3] |
| Solubilidade | miscível com etanol, glicerina e éter dietílico[4] |
| Pressão de vapor | 43 hPa (20 °C)[2] |
| Acidez (pKa) | 3,77[5] |
| Índice de refracção (nD) | 1.3694 [6] |
| Viscosidade | 1.57 cP at 26 °C [carece de fontes] |
| Estrutura | |
| Forma molecular | Planar |
| Momento dipolar | 1.41 D(gas) |
| Termoquímica | |
| Entalpia padrão de formação ΔfH |
-378.6 kJ/mol (gás) -425.1 kJ/mol (líquido) |
| Entropia molar padrão S |
248.7 J mol-1 K-1 (gás) 131.8 J mol-1 K-1 (líquido) |
| Capacidade calorífica molar Cp 298 |
45.7 J mol-1 K-1 (vapor) 99.0 J mol-1 K-1 (líquido) |
| Riscos associados | |
| MSDS | ScienceLab.com |
| Principais riscos associados |
Corrosive; irritant; sensitizer. |
| NFPA 704 | |
| Frases R | R10 R35 |
| Frases S | S1/2 S23 S26 S45 |
| Ponto de fulgor | 69 °C[1] |
| Temperatura de auto-ignição |
520 °C[1] |
| LD50 | 700 mg/kg (camundongo, oral) 145 mg/kg (camundongo, intravenoso) 940 mg/kg (camundongo, intraperitonial) [3] |
| Compostos relacionados | |
| Outros catiões/cátions | Metanoato de lítio Metanoato de sódio |
| Ácidos carboxílicos relacionados | Ácido acético Ácido propiônico Ácido carbônico |
| Compostos relacionados | Formaldeído Metanol Metanoato de metila Formamida |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
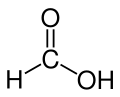
O ácido fórmico ou oficialmente ácido metanóico, CH2O2, de massa molecular 46 u, é um ácido monocarboxílico com fórmula estrutural H - COOH. É o mais simples dos ácidos orgânicos.
O nome fórmico tem sua origem do latim formica, que significa formiga, dado que a primeira vez que o ácido foi isolado ocorreu por destilação do corpo de uma formiga.
Propriedades
Físicas
- É um líquido incolor de cheiro irritante.
- Solúvel em água em qualquer proporção.
- Ponto de fusão: 8,4 °C
- Ponto de ebulição: 100,8 °C
Químicas
- Em solução aquosa libera 1 próton (H+), por molécula.
- Constante de ionização: 1,778 . 10−4.
- Grau de ionização: 4%
- Reage com álcoois produzindo ésteres.
- Reage com bases originando sais orgânicos.
Aplicações
- Como fixador de corantes em tecidos (mordente)
- Como acaricida
- Na medicina para o tratamento do reumatismo
- Obtenção de monóxido de carbono (CO)
- Produção de ácido oxálico (HCOO - COOH)
- Processamento de couro (acidificante na preparação para o curtimento do cromo e fixador de produtos aniônicos na etapa de acabamento molhado)
- Na coagulação do látex da borracha.
História e obtenção
- Desde o século XV alguns alquimistas e naturalistas já sabiam que formigas desprendiam um "vapor ácido".
- Inicialmente era extraído de formigas vermelhas (Formica rufibarbis), por destilação com vapor de água. Este processo foi desenvolvido pelo naturalista inglês John Ray, em 1671.
- Foi sintetizado pela primeira vez a partir do ácido hidrociânico pelo químico francês Joseph Gay-Lussac.
- Em 1855, outro químico francês, Marcellin Berthelot, desenvolveu um processo de síntese usando o monóxido de carbono, através de um processo bastante similar àquele que é usado atualmente.
- Industrialmente, é obtido em duas etapas a partir da reação de hidróxido de sódio com monóxido de carbono:
- NaOH + CO (150 °C e 8 atm. → H - COONa (metanoato de sódio)
- H - COONa + HCl → NaCl + H - COOH (ácido metanóico)
Ocorrência
- Nas abelhas, formigas, urtiga, pinheiro e em alguns frutos. O ácido é produzido e secretado para a finalidade de ataque e defesa.
Segurança
O ácido fórmico pode ser tóxico ao homem e ao meio ambiente e exige manipulação cuidadosa. Pode ser absorvido pelas vias oral, dérmica e inalatória, apresentando potencial para irritação local, e possivelmente, desenvolvimento de sintomas.[7]
No ambiente o ácido fórmico ocorre naturalmente como produto de biotransformação de reações metabólicas nos organismos vivos. O produto é facilmente biodegradável tanto na água quanto no solo. É prejudicial em organismos aquáticos, é nocivo para peixes e plânctons. Efeito prejudicial principalmente por alterar o pH do meio.[7]
O ácido fórmico pode ser irritante e corrosivo para a pele e mucosas, dependendo da sua concentração. Após exposição dérmica pode ocorrer acidose metabólica. Sintomas após a ingestão aguda (50 g ou mais) podem incluir salivação, vômito sanguinolento, sensação de dormência na boca, diarreia e dores severas. Após a exposição pode ocorrer colapso circulatório, depressão do sistema nervoso central e morte. A exposição constante (ocupacional) pode causar albuminúria e hematúria.[7]
O ácido fórmico apresentou-se mutagênico para Escherichia coli e células germinativas de Drosophila, porém não apresentou evidências de causar alterações no DNA de Bacillus subtilis em concentrações acima de 0,46%.[7]
Ecotoxicidade
- Toxicidade para peixes: Leuciscus idus CL50: 46 – 100 mg/L/96h[8]
- Toxicidade para algas: Desmodesmus subspicatus CL50: 27 mg/L/72h[8]
- Toxicidade para micro crustáceos: Daphnia magna CE50: 34,2 mg/L/48h[8]
- Toxicidade para bactérias: Pseudomonas putida CE50: 47 mg/L/17h[8]
| Riscos | |
|---|---|
| Ingestão | Dor de garganta, sensação de queimação no trato digestivo, dor abdominal, diarreia, vômitos. |
| Inalação | Sensação de queimação, tosse, dificuldade respiratória, perda de fôlego; sintomas de efeitos não imediatos. |
| Pele | Vermelhidão, dor, queimaduras cutâneas sérias. |
| Olhos | Dor, vermelhidão, visão turva, queimaduras profundas graves. |
| Unidades do SI são usadas quando possível. Salvo quando especificado o contrário, são considerados condições normais de temperatura e pressão. | |
Ligações externas
- ÁCIDO FÓRMICO - Ficha de Informações de Segurança de Produto Químico - COPENOR
- «Carbon monoxide as reagent in the formylation of aromatic compounds».
- «European Chemicals Bureau».
- «International Chemical Safety Card 0485».
- «NIOSH Pocket Guide to Chemical Hazards».
- «Computational Chemistry Wiki».
- «Formic acid dictionary-Guidechem.com».
Referências
- ↑ a b c ACIDE FORMIQUE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ a b Registo de CAS RN 64-18-6 na Base de Dados de Substâncias GESTIS do IFA.
- ↑ a b c d (en) « Formic acid » em ChemIDplus, consulté le 8 février 2009
- ↑ Thieme Chemistry, ed. (2009). RÖMPP Online - Version 3.5. Stuttgart: Georg Thieme Verlag KG
- ↑ «pKa Data Compiled by R. Williams (pdf)» (PDF). Consultado em 14 de abril de 2010. Arquivado do original (PDF) em 2 de junho de 2010.
- ↑ Yitzhak Marcus (1999). John Wiley & Sons Ltd, eds. The Properties of Solvents (em inglês). 4. England: [s.n.] 239 páginas. ISBN 0-471-98369-1
- ↑ a b c d HSDB – HAZARDOUS SUBSTANCES DATA BASE – TOXICOLOGY DATA NETWORK (TOXNET) – UNITED STATES NATIONAL LIBRARY OF MEDICINE (NLM).Formic acid
- ↑ a b c d ECOTOX - ECOTOXicology database – UNITED STATES ENVIRONMENTAL PROTECTION AGENCY (US EPA). «Formic acid». www.epa.gov.











