Evaporação
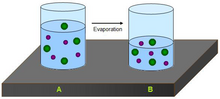
Evaporação é um fenômeno no qual átomos ou moléculas no estado líquido (ou sólido, se a substância se sublima) ganham energia suficiente para passar ao estado gasoso.
O movimento térmico de uma molécula de líquido deve ser suficiente para vencer a tensão superficial e evaporar, isto é, sua energia cinética deve exceder o trabalho de coesão aplicado pela tensão superficial à superfície do líquido. Por isso, a evaporação acontece mais rapidamente a altas temperaturas, a altas vazões entre as fases líquida e vapor e em líquidos com baixas tensões superficiais (isto é, com pressões de vapor mais elevadas).
Como apenas uma proporção pequena de moléculas está localizada perto da superfície e movendo-se na direção correta para escapar do líquido em um certo instante, a taxa de evaporação é limitada. Além disso, como as moléculas de maior energia escapam e as que ficam têm menor energia cinética média, a temperatura do líquido diminui. Este fenômeno também é chamado de resfriamento evaporativo. Um exemplo para tal fenômeno é a transpiração (suor). A evaporação promove resfriamento porque consome calor sensível e o transforma em calor latente, consumindo, no caso da água, cerca de 600 calorias por grama (600 quilocalorias por quilo) de água evaporada (inversamente, durante a condensação da água, ocorre a recuperação do calor sensível - também 600 calorias por grama).[1]
Equilíbrio evaporativo
Se a evaporação ocorrer em um recipiente fechado, as moléculas que escapam do líquido acumulam-se na forma de vapor acima do líquido. Muitas dessas moléculas, aliás, retornam ao líquido. Quando o processo de escape e retorno alcança um equilíbrio, o vapor é chamado de saturado, e não ocorrem mudanças adicionais na pressão de vapor ou na temperatura do líquido.
É um erro dizer que somente existe vapor de água a 100 °C a 1 atm. As moléculas de água estão em um estado constante de evaporação e condensação perto da superfície da água líquida. Se uma molécula na superfície da água recebe energia suficiente, ela deixará o líquido, com formação de vapor a uma certa pressão. A uma pressão de vapor de 1 atm, a água acaba fervendo, e isto ocorre a 100 °C.
A razão entre a perda de calor de uma superfície de água por evaporação e a perda de calor devido à convecção, independente da velocidade do vento, é dada por:[2]
onde é a perda de calor de uma superfície de água por convecção em W/(m²•K), é a perda de calor de uma superfície de água por evaporação em W/(m²•K), e são as temperaturas da água e do ar em Kelvin (ou Celsius) e e são as pressões de vapor da superfície da água e do ar e é a pressão barométrica, com todas as pressões em mmHg (Bowen, 1926).
Fatores que afetam a taxa de evaporação
- A concentração da substância evaporante no ar. Se o ar contiver uma alta concentração da substância que evapora, então tal substância evaporará mais devagar.
- A concentração de outras substâncias no ar. Se o ar já estiver saturado com outras substâncias, poderá ter uma capacidade menor para a substância que evapora.
- Temperatura. Se a substância estiver quente, a evaporação não será mais rápida. O fator chave que determina a rapidez com que o líquido pode evaporar não é a diferença de temperatura entre a superfície e o líquido, mas sim a diferença de pressão entre a superfície do líquido e o vapor ambiente.[3]
- Pressão. A evaporação é mais rápida se menos pressão é exercida sobre a superfície, a qual dificulta o escape das moléculas.
- Superfície de contato. Para volumes iguais uma substância que possua uma superfície de contato maior evapora mais rapidamente, pois há mais moléculas na superfície por unidade de volume que são potencialmente capazes de escapar.
- Vazão de ar. Isto está em parte relacionado com o tópico da concentração citado anteriormente. Se existe ar fresco passando pela substância o tempo todo, então é mais provável que sua concentração não aumente, o que favorece uma evaporação mais rápida. Além disso, moléculas em movimento têm mais energia cinética do que aquelas em repouso; por isso, quanto mais forte o fluxo de ar, maior é o potencial para evaporação.
- Forças intermoleculares. Quanto maiores as forças intermoleculares dentro do líquido ou sólido, mais energia será necessária para fazer suas moléculas evaporarem.
Aplicações da evaporação
Evaporações forçadas
É um processo usado na separação de misturas, no qual uma mistura é aquecida de forma a promover a evaporação do componente mais volátil (por exemplo, água) e deixar sobrar o componente menos volátil (por exemplo, sal).
Deposição de filmes
A evaporação é um método comum de deposição de filmes finos, usada na indústria. A deposição evaporativa é um processo geralmente mais lento e, por isso, mais caro do que o método por impacto de íons. Contudo, substratos plásticos geralmente não podem tolerar o bombardeio com átomos energeticamente neutros que inevitavelmente surgem em uma câmara de sputtering.
Para algumas aplicações, o fato de a deposição evaporativa ocorrer de modo diretamente visual (line-of-sight fashion, em inglês) é uma vantagem importante. A distribuição de energia do material evaporado aproxima-se a uma distribuição maxwelliana, com a temperatura da fonte de evaporação. Em contraste, os encontrados nos sistemas de sputtering estão longe do equilíbrio térmico e podem ter a distribuição desviada para o lado de maior energia, ou seja, têm partículas com velocidades aleatórias maiores. Por isso, a evaporação é um processo mais suave, com um feixe mais bem definido de matéria-prima que pode ser usado para revestir apenas um lado de um substrato ou até mesmo o lado característico de superfícies gravadas, como no processamento MEMS.
Os três principais tipos de evaporação são térmica, por feixe de elétrons e resistiva. No método térmico, o cadinho que retém a matéria-prima é aquecido por irradiação por um filamento que o envolve. No método por feixe de elétrons, a corrente que aquece o cadinho é proveniente de um filamento e atraído ao cadinho por alta voltagem. A evaporação resistiva é feita pela passagem de uma grande corrente através de um fio ou lâmina do material a ser depositado.
Referências
- ↑ Francisco Mendonça e Inês Moresco Danni-Oliveira, Climatologia - Noções Básicas e Climas do Brasil, página 58, 2007, Editora Oficina de Textos
- ↑ I. S. Bowen (1926). «The Ratio of Heat Losses by Conduction and by Evaporation from any Water Surface». Physical Review. 26: 779–787
- ↑ The physics of evaporation explained Changes in pressure, more so than temperature, strongly influence how quickly liquids turn to gas, researchers show. por Amit Malewar (2019)
















